등록일2015-02-05
Palbociclib, 유방암 치료제로 새로운 장을 열다.
최근 CDK(cyclin-dependent kinase)4/6 저해제인 Palbociclib (상품명: Ibrance)가 FDA로부터 허가 승인을 받았다. 전이성 유방암 환자를 대상으로 임상 2상만을 마치고 결정시기를 2개월이나 앞당겨 허가를 받은 것이다. FDA oncology chief인 Richard Pazdur는 기존 치료제 대비 획기적인 치료제에 대하여 신속허가에 대한 의지를 보여준 것으로 보인다.
Estrogen receptor 양성 환자 치료의 한계
Estrogen receptor 양성(이하 ER+로 기재) 환자는 anti-estrogen으로 치료가 가능하나 반응률이 낮거나 내성이 생기는 문제가 있다. 이 문제의 해결책으로 HER1, HER2 pathway, angiogenesis, IGFR를 대상으로 치료법이 개발되었으나 성공하지 못하였고, mTOR 저해제인 everolimus가 유일한 성공 케이스였다. ER+인 luminal type은 세포 분열을 활발히 하는 암 종으로, cell cycle 조절을 통한 항암 효과를 기대해 볼 수 있었던 것이다. 하지만 CDK 저해제는 독성 문제를 안고 있어 개발이 용이하지 않았다.
Estrogen receptor 양성 및 HER2 음성 환자를 대상으로 임상
허가 승인의 근거가 된 PALOMA-1 임상에서는 Palbociclib + letrozol (Aromatase inhibitor, 상품명 Femara)와 병용으로, 그리고 letrozol 단독으로 2상을 완료하였다. 공개, 무작위배정으로 진행된 이 임상은 Estrogen receptor(ER) 양성, HER2 음성 (이하 HER2- 로 기재) 이며 이전에 systemic 치료를 받지 않은 165명의 폐경기 여성 환자를 대상으로 진행하였다.
추가로 군을 2개로 나누었으며 cohort 1은 ER+, HER2- biomarker만 있는 군 (n=66), cohort 2는 ER+, HER2-, cyclinD1이 증가 혹은 p16이 결여된 군이었다. (CDK4의 역할에 관계되는 단백질의 biomarker로 가능성을 보기 위함.) (n=99).
처방 용량은, 단독 letrozol 2.5 mg (n=84) 과 병용 letrozol 2.5mg + pabociclib 125 mg (n=81)을 3주 매일 복용 후 그리고 1주를 쉬는 28-day cycle로 진행하였다.
표 1. Patient profiles of PALOMA-1 trials
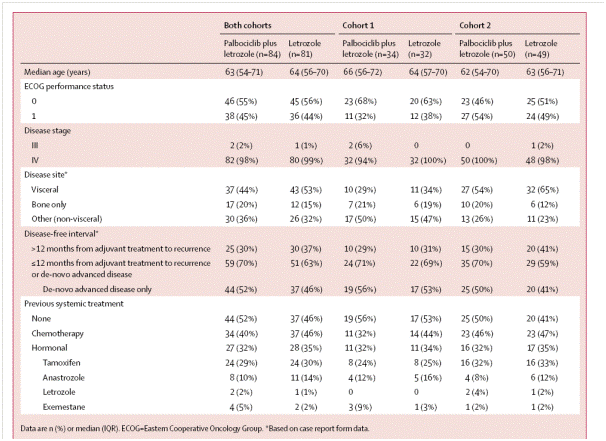
2009년 12월22일부터 2012년 5월 12일까지 진행된 결과에 의하면
letrozol군은 27.9개월, letrozol과 palbociclib 병용군은 29.6개월을 관찰하였다.
표2. Letrozol 단일집단과 pabociclib 병용집단의 생존기간
|
|
관찰기간 |
PFS event |
Median PFS |
Overall Survival |
|
Letrozol |
27.9 개월 |
41건 |
10.2개월 |
33.3 개월 |
|
Letrozol +palbociclib병용 |
29.6 개월 |
59건 |
20.2 개월 |
37.5 개월 |
Harzard ratio=0.488 95% CI 0.391-0.748, one-sided p=0.0004
Cohort 1에서는 letrozol의 PFS는 5.7개월, palbociclib병용군의 PFS는 26.1개월이었으며 (HR=0.299, 0.156-0.572, one sided p<0.0001), Cohort 2에서는 letrozol 단독군의 PFS는 11.1개월, palbociclib병용군의 PFS는 18.1개월이었다. (HR=0.508, 0.303-0.853, one-sided p=0.0046)
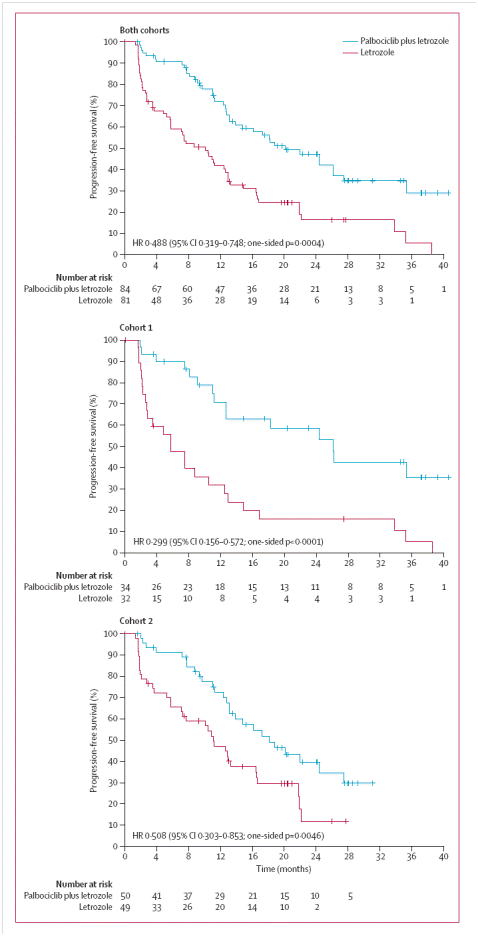
그림1. Progression-Free Survival of cohorts in Pablociclib+letrozol and letrozol only.
Biomarker cyclinD1 증가, p16억제된 환자군(Cohort 2)은 선택에 사용될수 있을까를 보았지만 결과는 그렇지 않다고 나왔다. 그래서 ER+가 현재로서는 최선의 치료 대상으로 보인다. CDK4/6의 역할은 Rb에 의존하므로Rb-negative또한 치료 대상으로 고려 되어야 하는데 ER+환자에서 Rb-negative는 드물게 있다.
또한 종양이 줄어든 비율을 평가하는 종양반응율 에서도 표3과 같이 palbociclib 병용 그룹에서 더 많은 환자가 개선 효과를 나타내었다.
표3. Best overall response in PALOMA-1 trials
안전성 측면에서는 위 약물의 가장 흔한 부작용으로 neutropenia가 있으나 치료가 가능한 수준이다. palbociclib은 marrow progenitor cell에 세포독성이 있기보다는 세포 분열 억제제로서, 일반 독성이 있는 항암제와는 다른 성향을 띈다.
표4. Common side effects in palbocilclib administration
Pablocilclib의 약물 내성 가능성?
FDA도 치료가 필요한 곳에서는 융통성을 보여 허가를 일찍 내줄 수도 있다는 의지를 보인 좋은 예이다. ER+는 유방암에서 환자가 많음에도 불구하고 hormone 억제제가 대세를 이루면서 내성이 있는 환자에 대한 치료법이 개발되지 않았던 면에서 medical unmet need가 많은 부분이었다. CDK4/6 inhibitor는 이 환자 군에서 좋은 효과를 내어 FDA를 설득시키기에 충분했던 것으로 보인다. 하지만 이 치료제 또한 약물 내성을 보일 것으로 전망된다.
한올바이오파마는 biguanide 계열 화합물을 개발 중에 있다. 이 biguanide 계열의 화합물은 항암제의 약물 내성을 치료할 수 있는 가능성을 제시하고 있기에, 많은 항암제 내성을 앓고 있는 환자를 위한 좋은 소식을 전해 줄 수 있을지 기대한다.
근거]
Finn RS et al (2015) Lancet 16. 25-35 The cyclin-dependent kinase 4/6 inhibitor palbociclib in combination with letrozol alone as first-line treatment of oestrogen receptor-positive, HER2-negative, advanced breast cancer (PALOMA-1/TRIO-18): a randomized phase 2 study